Diagnosticul bolilor ereditare
Diagnosticul clinic al bolilor ereditare să țină seama de caracteristicile lor comune:
- existența unor cazuri similare în familie și între rude îndepărtate;
- recidivante, cronice, tratamentul pe termen lung pentru bolile greu de rezolvat;
- prezenta simptomelor specifice rare sau combinații ale acestora;
- eșecul multor organe și sisteme;
- prezența a mai mult de 5 variante morfogenetice congenitale, numite microanomalies semne de dezvoltare disembriogeneza, semne de displazie, stigmate, care sunt în afara structurii normale a corpului de variație, dar spre deosebire de malformații nu violează funcționarea organelor;
- natura înnăscută a bolii.
În cazul în care un astfel de studiu diagnostic precis nu este suspectat și este o boală ereditară, pentru a diagnostica folosind metode genetice speciale.
studiu detaliat de familie clinice genealogie și, uneori, poate detecta tiparele de moștenire a unor simptome.
Examinarea citogenetica. Indicații pentru reuniune sunt după cum urmează:
- suspiciune de boală cromozomial;
- malformații congenitale multiple;
- mai multe rezultate negative sarcinii (avort spontan, nasterea unui copil mort, malformațiilor congenitale în dezvoltarea copiilor);
- tulburări de reproducere;
- diagnostic prenatal.
Metodele moleculare genetice permit diagnosticarea bolilor ereditare la nivelul ADN-ului (gene). Toate multele variante ale acestor metode sunt bazate pe tehnici de tehnologia ADN-ului recombinant sau inginerie genetică.
Metodele biochimice sunt folosite în boli metabolice ereditare suspectate. Acestea pot fi în mai multe etape ( „program de screening“) sau doar ca scop strict la o anumită patologie. Diagnosticul biochimic, folosind toate tehnicile moderne de biochimie.
inspecția imunogenetice a pacientului, rudele sale dezvăluie imunodeficiențe ereditare, utilizați datele pentru a diagnostica de gena ambreiaj, pentru a evalua compatibilitatea mamei și a fătului pentru a determina prognosticul bolilor cu predispoziție ereditară.
Metodele citologice sunt utilizate în diagnosticul diferențial al bolilor de piele, boli de stocare (mucopolizaharidoze, Mucolipidosis).
Metoda de cuplare a genei este recomandată în cazurile în care diagnosticul directă posibil. Aceasta rezolvă problema dacă probandului moștenit gena mutant, în cazul în care există un pedigree boală. Metoda se bazează pe modelul de gene comune de transmisie genetice localizate într-un cromozom (grup de legătură).
Principiile tratamentului bolilor ereditare. Având în vedere diversitatea tipurilor de mutații care perturbate de unități de schimb, implicarea organelor și sistemelor pot să nu fie identice metode de tratament pentru diferite forme de boli ereditare. În centrul tratamentului lor sunt utilizate, precum și în alte zone boli - simptomatic, patogenic, etiologic.

instrucțiuni de ghidare simptomatici și patogenice includ utilizarea tuturor tipurilor de tratament moderne: medicamente, dieta, chirurgie, radiologie, fizioterapie. Recuperarea completă în cazul bolilor ereditare nu este încă posibilă, dar tratamentul lor - nu un astfel de program fără speranță din punct de vedere terapeutic, așa cum părea înainte.
Tratamentul simptomatic este prescris în aproape toate bolile ereditare, și este singura cale pentru mai multe forme. În plus, consolidează efectul pozitiv al tratamentului patogenetic. Tipuri de tratament simptomatic divers - de la medicamente la corecție chirurgicală.
Terapia patogenetic îndreptate spre corectarea unităților metabolice depreciate. În cazul în care gena nu funcționează, este necesar să se compenseze produsul; dacă gena produce sunt formate proteine anormale și produse toxice, acestea trebuie îndepărtate și compensează funcția de bază a genei; dacă gena produce o mulțime de produs, excesul este eliminat.
În practica clinică, se folosesc din ce în ce următoarele forme de terapie patogenetic:
- dieta restrictivă specifică, cum ar fi limitati aportul fenilketonurie de fenilalanină din alimente (copil transferat la hrănirea artificială); la galactozemie exclud galactoză, boala Refsum - acidul fitanic;
- eliminarea metaboliților anormale din corp. hemocromatoza primar, de exemplu, tratate prin bloodletting repetate. produse metabolice intermediare Acumulate pot fi eliminate cu medicamente, dializa de sange, haemo- si lymphosorption;
- înlocuirea produsului lipsă (globulină antihemofilic in hemofilie A, hipotiroidism, hormoni tiroidieni, hidrocortizon la sindromul adrenogenital);
- inducție enzimatică (folosind doze mici de Fenobarbital în unele forme de hiperbilirubinemie);
- cofactor de compensare (în cazul în care statele vitaminzavisimyh);
- excluderea de medicamente care cauzează un efect patologic in purtatori ai genei mutante (de exemplu, anti-malarie sau sulfamide medicamente cu deficit al enzimei G-6-PDG);
- transplantul de organe și țesuturi.
Tratamentul etiologic care vizează repararea gena sau suprimarea activității sale, numită terapie genică. Segmentul de ADN clonat este o genă sau o parte activă, împreună cu regiunile de reglementare sunt inserate în vectori și introduși în celule. Transferul vectorilor sau segmente de ADN donate în celule este posibilă prin microinjecție directă, electroporare, mediată chimic transfecție folosind virusuri. Această procedură se numește transgenic. Acțiuni de închidere de funcționare a genei mutante este posibil prin diferite tipuri de suprimare a ARN-ului.

demonstrat experimental doua tipuri de terapie genica - folosind un transgenice de celule germinale și somatice.
inginerie genetică tratament prin celule somatice transgenice. Transferul de gene în celule somatice poate fi efectuată ex vivo și in vivo. Luate din celulele organismului ale maduvei hepatice, osoase, limfocitele pot fi supuse necesare materialului genetic transgenice și returnate organismului, în cazul în care acestea compensează defect ereditar. Un astfel de tratament este deja aplicat în imunodeficiențe combinate, cauzata de mutatii in gena pentru adenozin dezaminază (limfocite), boala Gaucher (măduvă osoasă), hipercolesterolemie familiala (celule hepatice).
Este de asemenea posibil transgeneză directă, și anume in vivo, când vectorul cu gena construct predeterminate obiective celulele țintă din organism.
O astfel de abordare a fost deja testate pentru tratamentul fibrozei chistice. gena adenoviral vector transmembranar regulator cu ioni de sodiu (mutatie in aceasta gena duce la fibroza chistica), este introdus prin caile respiratorii superioare, unde pătrunde celulele epiteliale. Produs de proteine gena introdus normalizează transportul ionilor de sodiu prin epiteliul mucoasei.
Posibilitatea de terapie genica pare a merge dincolo de tratament doar de boli ereditare. În prezent, numeroase studii realizate pentru a dezvolta metode pentru tratamentul neoplasmelor maligne, infecții virale, în special SIDA, folosind diferite abordări ale terapiei genice.
In dezvoltarea tehnicilor de terapie genică și aplicarea lor sunt acordând o atenție deosebită securității, atât pentru pacient cât și pentru mediul înconjurător, la fel ca în laborator pentru a crea noi genetice „structură“, nu întâlnite anterior în natură. Siguranța biologică a terapiei genice este reglementată de reglementare relevante (legislativă) acționează și comitetele de bioetică la nivel național și internațional. Toate tipurile de terapie genică sunt testate riguros pentru eficacitatea și siguranța, inclusiv condițiile care se aplică la testarea medicamentelor.
Există următoarele domenii de prevenire a bolilor ereditare:
- 1) Planificarea familială (prevenție primară);
- eliminarea embrionilor patologice și fetușilor (prevenția primară);
- penetranta și control expresivității (prevenție secundară);
- mediu (prevenirea primară și secundară).
Familie de planificare din punct de vedere genetic se face prin consiliere genetică. Acest tip de îngrijire terțiară, de fapt, trebuie să fie disponibile pentru fiecare familie a unui copil bolnav de naștere (consultanță prospectiv) și, desigur, este obligatorie după nașterea unui copil bolnav (consultanță retrospectivă). Prezența pacienților în pedigree-ul este, de asemenea, o indicație directă pentru consiliere genetică. Medic-genetician, împreună cu specialiștii de diagnostic clinic, având în vedere rezultatele studiilor de laborator de genetică (citogenetice, biochimice, imunologice, molecular-genetice), a declarat că situația genetică în familie și dă un aviz cu privire la riscul de re-nașterea copilului bolnav și nevoia de diagnostic prenatal.
Riscul nu depășește 10%, se referă la cel mai mic, cu fertil nu poate fi limitat. Riscul de 10 la 20% este considerat un risc pentru valoarea medie. În aceste cazuri, planificarea nașterilor este necesar să se țină seama de gravitatea bolii și durata de viață a copilului. Mai grea a bolii, și cu cât viața copilului bolnav, cu atât mai mare restricțiile cu privire la re-nașteri.
La un risc ridicat de a avea un pacient copil (20% sau mai mare) să se abțină de la reproducerea ulterioară. Astfel, toate moștenirea (nu sporadice), cazurile de un copil cu o boală dominantă și recesivă sunt expuse unui risc ridicat de re-nașterea unui copil bolnav.
Decizia de a concepe, diagnostic prenatal sau la nastere, desigur, ia familia, mai degrabă decât medic-genetician. Sarcina medic-genetician - pentru a determina riscul pacientului de naștere a copilului și a familiei pentru a explica esența recomandărilor, care nu ar trebui să fie prescriptive, și pentru a ajuta la a face o decizie.
Indicații pentru consilierea genetică sunt:
- suspiciunea unei patologii ereditare sau congenitale (diagnostice sau diagnostice diferențiale);
- prezenta bolii genetice la un pacient (flux prognosticul bolii);
- modificări ale funcției reproductive la femei și bărbați (infertilitate primara tulburari ale ciclului ovarian, dezvoltarea anormală a organelor de reproducere, avorturi spontane recurente, stillbirths.);
- nașterea unui copil cu malformatii congenitale sau boli genetice (prognozarea boli ereditare la copii nenăscuți);
- prezența în familie de boli ereditare (predictia bolii la rude sau copii sănătoși viitoare);
- vârsta soților (în vârstă de peste 35 de femei, bărbați peste 45 de ani) planificarea nașterilor;
- căsătorie de rudenie (de până la trei ori frați eliminate);
- chimice mutagene și expunerea la radiații.

Consilierea genetică în România sunt deținute în consiliere genetică, organizat, de obicei, în spitale regionale și municipale. Astfel de consultări sunt disponibile și la clinici universitare, precum și institute de cercetare. In plus fata de geneticieni medicale si asistente medicale, personalul biroului este format din geneticienii de laborator care efectuează diagnosticul citogenetic și biochimic al bolilor ereditare.
Eliminare a embrionilor și fetușilor patologice (avort) se efectuează după diagnostic prenatal, care este în prezent cea mai comună metodă de prevenție primară. Diagnosticul prenatal se efectuează după consiliere genetică. Metode de diagnostic prenatal sunt împărțite în invazive și non-invazive.
Pentru non-invazive metode includ ultrasunete. Dezvoltarea intarziata a embrionului si fatului este posibila cu boli ereditare, care pot fi detectate cu 8-10 săptămâni de gestație. Pe de 18-24 săptămâni lea de sarcină, examinare cu ultrasunete dezvaluie multe defecte congenitale si ereditare - reducerea membrelor, anencefalia, hernie spinării.
Pentru metode non-invazive includ un studiu de alfa-fetoproteinei, gonadotropina corionică umană, estriol neconjugat în serul gravidă. In prezenta fetale spinării hernie, anencefalia sau concentrare sindromul Down a acestor substanțe este schimbat (una - este crescută, altele - este redusă). Aceste metode sunt aproximative, denumite uneori sitare (sortare).
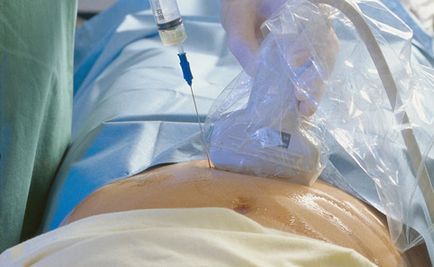
Metodele invazive permit diagnosticarea bolii cu exactitate. Esența lor este împușcat celule (sau tesuturi) ale fatului pentru studiul citogenetic, biochimice, moleculare genetice, morfologice in care toate bolile cromozomiale diagnosticate si aproximativ 400 de boli ale genei.
Celulele (sau țesut) ale fătului luate în moduri diferite și în diferite stadii ale sarcinii:
- biopsie (sau aspiratie) sau placenta corionica - 7-11 Săptămâna;
- Amniocenteza si prelevarea de probe de celule din lichidul amniotic - 15-16 săptămâni;
- cordocenteza și prelevarea de probe de sânge fetale - 18-22 Săptămâna;
- biopsie de piele, mușchi - 16-22 Săptămâna.
Advances in genetica moleculara au permis sa inceapa dezvoltarea de diagnostic pre-implantare. Prin fertilizarea in vitro, la stadiile de clivaj timpurii (8-18 celule), separate de 1-2 celule, care pot fi diagnosticate.
Indicații pentru diagnostic prenatal sunt:
femei cu varsta de peste 35 de ani, bărbații de peste 45 de ani;
avand un copil cu cromozomiale sau boli genetice;
prezența unei translocatie echilibrate în oricare dintre părinții lor;
heterozigoției ambilor părinți asupra genei bolii.
Diagnosticul prenatal se realizează în România numai câteva orașe mari (București, București, Tomsk, Voronezh).
Controlul penetranta și expresivității se bazează pe cunoașterea patogenezei bolii și în aplicarea așa-numitul tratament preventiv. Esența unei astfel de management se reduce la detectarea preclinice a pacienților și a tratamentului lor preventiv.
Screening (screening) program pentru a identifica boli ereditare la nou-născuți sunt utilizate în prezent pentru diagnosticul de fenilcetonurie, hipotiroidism și sindromul adrenogenital. În unele țări, este diagnosticat ca galactosemie. Când fenilcetonuria și copilul galactosemie transferate respectiv besfenilalaninovuyu sau dieta bezgalaktoznuyu. In hipotiroidism sau sindromul adrenogenital prescris terapia hormonală de substituție.
Metodele de prevenire a preconceptie. instruirea corespunzătoare a mamei (cum ar fi fortificație) înainte de concepție și la începutul sarcinii reduce probabilitatea de a avea un copil cu defecte congenitale.
detectare preclinice a alelei transportatorilor tăcut ", își exercită efectul patologic numai sub influența anumitor factori, face posibilă prevenirea patologiei prin eliminarea factorilor„permisive“(mai ales droguri).
De mediu, facilitează atât prevenția primară și secundară. mutageni Excepție (adesea ele sunt atât cancerigeni, teratogens și) din habitatul uman reduce procesul de mutație și deci frecvența bolilor ereditare datorate noi cazuri. Metodele de testare a factorilor de mediu asupra mutagenitate. Utilizarea lor ar trebui să fie obligatorie pentru medicamente, aditivi alimentari, pesticide și alte substanțe chimice utilizate în mod obișnuit în mediu sistem de factorii de mediu igienic.