legătură chimică din metal 1
scop
- Da o idee despre legătura chimică a metalului.
- Aflați cum să scrie formarea de circuit a legăturii metalice.
- Familiarizat cu proprietățile fizice ale metalelor.
- Aflați cum să facă o distincție clară între tipurile de legături chimice.
obiectivele lecției
- Aflați cum să interacționeze atomii de metal
- Determina cum să influențeze legătura metalică formată pe proprietățile materialelor sale
Termeni cheie:
- Electronegativitate - proprietate chimică a unui atom, care este o caracteristică cantitativă a abilității unui atom dintr-o moleculă pentru a atrage perechilor de electroni partajate.
- Chimică lipirea unui fenomen de interacțiune al atomilor, datorită suprapunerii norilor de electroni ai atomilor care interacționează.
- bond metal - o legătură simplă între atomii din metale și ioni formate datorită schimbului de electroni.
- Legătură covalentă - legătura chimică formată prin perechile suprapuse de electroni de valență. Furnizarea de electroni Feedback sunt numite pereche de electroni totală. Este de 2 tipuri de polare și nu polare.
- Ionic legătură - legătura chimică care este formată între atomi nemetalov unde perechea de electroni totală merge la atomul cu electronegativitate mai mare. Ca urmare, atomii sunt atrase ca organisme încărcate opus.
- legături de hidrogen - legătura chimică dintre un atom electronegativ și un atom de hidrogen H, legat covalent la un alt atom electronegativ. Ca un atomii electronegative poate servi N, O sau F. legături de hidrogen pot fi intramoleculare sau intermoleculare.
legătură chimică de metal
Să identifice elementele care au devenit nu este „Cumpăna“ .Pochemu?
Ca Fe P K Al Mg Na
Care sunt elementele din tabelul periodic sunt numite metale?
Astăzi, știm care au proprietăți metale, și ele depind de conexiunea care se formează între metale yonami.
În primul rând, să mestoraspolazheniya metale din tabelul periodic?
Fier așa cum știm cu toții, nu sunt de obicei sub formă de atomi izolați, și sub forma unei piese, lingou sau produse din metal. Clarificarea care colectează atomii de metal din întregul ecran.

Fig. 1. Aur.
Pe exemplul vom vedea o bucată de aur. Si apropo de metal unic este de aur. Cu forjare de aur pur poate fi folie de grosime de 0,002 mm! o foaie de folie nonchayshy aproape transparentă și are un lumen tentă verde. Ca urmare a aurului Nuggets marimea unei cutii de chibrituri poate fi obținută o folie subțire, care va acoperi zona unui teren de tenis.
Punct de vedere chimic, toate metalele sunt caracterizate prin ușurința întoarcere a electronilor de valență, și în consecință formarea ionilor încărcați pozitiv și să fie numai oxidare pozitivă. Acesta este motivul pentru care metalele sunt într-o stare liberă Studio de rețea. O trăsătură comună a metalelor sunt atomi de mari dimensiuni în raport cu nemetalam. ellektrony extern situat la distanțe mari de nucleu, și, prin urmare, slab asociat cu ea, atât de ușor să vină off.
Atomii de cantități mari de metale la nivel extern au puține număr surprinzător de mare de electroni - 1,2,3. Acești electroni ușor detașat și atomii de metal devin ioni.
Me0 - n e ⇆ Men +
atomii din metal - E-Ext. orbită ioni metalici ⇆
Astfel peremeschatsya poate desprinde electroni de la un ion la altul Ie deveni liber, și cum ar fi legarea lor într-un singur tseloe.Poetomu Se pare că toți electronii se desprinde evlyaetsya generală, deoarece este imposibil să înțeleagă cum ellektron aparține atomii de metal.
Electronii poate fi unit cu cationi, în timp ce temporar atomii sunt formate, din care const apoi detașat electroni. Acest proces are loc în mod continuu și fără întrerupere. Se dovedește că volumul atomilor metalici devin ioni în mod continuu și vice-versa. Când acest număr mic de electroni partajate leagă un număr mare de atomi de metal și ioni. Dar este important ca numărul de electroni din metal este egală cu sarcina totală a ionilor pozitivi, adică se pare că, în general, metalul rămâne neutru electric.
Acest proces este reprezentat ca un model - ionii metalici sunt într-un nor de electroni. Un astfel de nor de electroni numit „gaz de electroni“.
Aici, de exemplu, în această imagine vom vedea modul în mișcare elektronchiki printre nepodvizhnyhyonov în interiorul rețelei de cristal-metal.
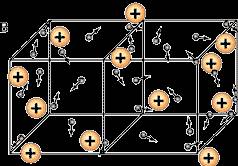
Fig. 2. Mișcarea de electroni
Acum putem scrie definiția: legătura metalică - o legătură în metale între atomii și ionii sunt formate prin schimbul de electroni.
Liantul metalic este nu numai metalele pure, ci și caracteristică amestecuri de diferite metale, aliaje în diferite stări de agregare.
Liantul metalic este importantă și determină proprietățile de bază ale metalelor
- conductivitate - mișcare E-aleatoare în metal în vrac. Dar când o diferență de potențial mic. electronii se deplasează ordonat. Cu mai bune metale conductivității sunt Ag, Cu, Au, Al.
- ductilitate
Conexiunile dintre straturile de metal nu sunt foarte semnificative, permite să se deplaseze straturile sub sarcină (deforma metalul fără a rupe-l). Metale deformabile Top (moale) Au, Ag, Cu.
- luciu metalic
Electron de gaze reflectă aproape toate razele de lumină. De aceea, atât de mult metalele pure strălucească și de multe ori au senryu sau alb. Metalele sunt cele mai bune reflectoare Ag, Cu, Al, Pd, Hg
Exercitiul 1
Selectați compușii care au formula
a) o legătură covalentă polară: Cl2, KCl, NH3, O2, MgO, CCl4, SO2;
b) cu o legătură ionică: HCl, KBr, P4, H2S, Na2O, CO2, CaS.
Exercitiul 2
Taie inutile:
a) CuCl2, Al, MGS
b) N2, HCI, O2
a) Ca, CO2, Fe
g) MgCl2, NH3, H2
Interesant de știut că ...
sodiu metalic. litiu metalic, și alte metale alcaline variază de culoare flacără. litiu metalic și o sare a acestuia conferi --krasny culoare flacără, sodiu metalic și sodiu - galben potasiu metalic și sărurile sale - violet, și rubidiu și cesiu - și violet, dar mai ușoare.

Fig. 4. O bucată de metal litiu
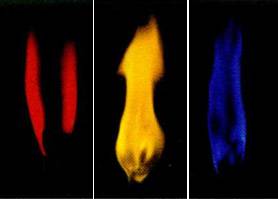
Fig. 5. Metale Colorare flacără
Litiu (Li). Metalul de litiu ca sodiu metalic, un metal alcalin. Ambele sunt solubile în apă. Sodiu, dizolvat în apă formează un acid foarte puternic sodă caustică. La dizolvare metale alcaline în apă multă căldură și gaz (hidrogen). Astfel de metale, este de dorit să nu se atingă, pentru că puteți obține ars.
Referințe
Editat și a trimis Lisnyak AV
Mai sus lecția a lucrat:
Ridicați problema educației moderne, pentru a exprima o idee sau pentru a rezolva problema în picioare, puteți la Forumul Educațional. în cazul în care educația internațională va bord cu gânduri și acțiuni proaspete. Prin crearea unui blog, va spori nu numai statutul său ca un instructor calificat, dar, de asemenea, aduce o contribuție semnificativă la dezvoltarea școlii viitoare. Liderii Alianței Educație își deschide porțile pentru profesioniștii din cel mai înalt rang, și invită să coopereze pentru crearea celor mai bune școli din lume.